国立保健医療科学院 生活環境研究部
上席主任研究官 志村 勉
E-mail:simura.t.aa(AT)niph.go.jp
広島大学原爆放射線医科学研究所
教授 笹谷 めぐみ
E-mail:mtoyosh(AT)hiroshima-u.ac.jp
※(AT)は半角@に置き換えてください。
国立保健医療科学院 生活環境研究部の志村 勉 上席主任研究官、牛山 明 部長らの研究グループは、広島大学 原爆放射線医科学研究所(分子発がん制御研究分野)の笹谷 めぐみ 教授らと共同で、放射線被ばくによるミトコンドリア損傷が炎症反応を誘導する分子機構を明らかにしました。
本研究では、正常ヒト線維芽細胞及びマウスモデルを用い、放射線によって生じたミトコンドリア損傷により、ミトコンドリアDNA(mtDNA)が細胞質へ放出される現象に着目しました。その結果、漏出したmtDNAが細胞内DNAセンサーであるcGASに認識され、STING経路を介した炎症反応が活性化されることを示しました。
さらに、このmtDNAは細胞内に留まらず、エクソソームや血中遊離DNAとして体内を循環し、放射線被ばく後の全身性炎症反応に関与する可能性が示唆されました。
本研究成果は、英国科学誌 『Scientific Reports』 にオンライン掲載されました
s41598-025-04845-0
<発表論文>
論文タイトル
Ionizing radiation triggers the release of mitochondrial DNA into the cytosol as a signal of mitochondrial damage
著書
Tsutomu Shimura*, Yui Takahashi, Chihiro Saito, Riko Maida, Megumi Sasatani, Tatsuki Kunoh, Akira Ushiyama
*責任著者
掲載雑誌
Scientific Reports
DOI:10.1038/s41598-025-04845-0
s41598-025-04845-0
放射線による発がんリスク評価は、主に疫学データに基づいて行われていますが、低線量・低線量率被ばくにおける生体影響の分子基盤には未解明な点が多く残されています。
近年、がんの発生・進展において慢性炎症が重要な役割を果たすことが明らかになっており、放射線による炎症誘導メカニズムの理解は、放射線発がんの本質を理解するうえで重要です。
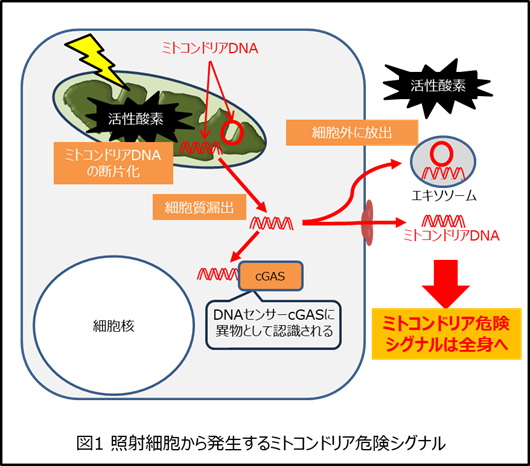
放射線被ばく後、正常ヒト線維芽細胞において3時間以内に細胞質内DNAが検出され、その状態が1週間以上持続することを確認しました。細胞質DNAの約半分はミトコンドリアDNA(mtDNA)(注1)であることが分かりました。mtDNAの漏出は、活性酸素(ROS)依存的に誘導され、細胞老化(セネッセンス)と強く関連していました。細胞質に漏出したmtDNAは、cGASおよびリン酸化STINGと共局在し、炎症シグナルを活性化していました(注2)。マウス全身被ばくモデルにおいても、血中リンパ球や血漿中にmtDNAが検出され、エクソソーム(注3)や遊離DNAとして全身に広がることが示されました。
本研究により、ミトコンドリア損傷に由来するmtDNAが放射線被ばく後の炎症反応を駆動する主要なシグナルであることが明らかになりました。
これらの知見は、放射線発がんの分子機構解明、低線量被ばく影響の科学的理解、放射線被ばくに対する健康不安や風評被害の軽減に貢献することが期待されます。今後は、低線量・低線量率被ばく条件下での検証や、炎症制御を標的とした新たな放射線防護・介入戦略への応用が期待されます。
注1) ミトコンドリアDNA(mtDNA):ミトコンドリアに存在する独自のDNA
注2) cGAS/STING経路:細胞質DNAを感知し炎症反応を誘導する自然免疫シグナル経路
注3) エクソソーム:細胞間情報伝達を担う微小小胞
国立保健医療科学院 生活環境研究部
上席主任研究官 志村 勉
E-mail:simura.t.aa(AT)niph.go.jp
広島大学原爆放射線医科学研究所
教授 笹谷 めぐみ
E-mail:mtoyosh(AT)hiroshima-u.ac.jp
※(AT)は半角@に置き換えてください。
掲載日 : 2026年02月04日
Copyright © 2003- 広島大学