TEL: 082-257-5280
FAX: 082-257-5284
E-mail: sugi*hiroshima-u.ac.jp (注: *は半角@に置き換えてください)
本研究成果のポイント
- チロシナーゼという酵素は、活性化すると肌のシミの原因となるメラニンを生成しますが、その酵素反応機構については明らかにされていませんでした。
- 分光学的解析法とX線結晶構造解析法を駆使して、チロシナーゼの反応機構の詳細な解明に世界で初めて成功しました。
- 今回の結果は、機能性の高い酸化酵素や低分子触媒の開発に役立てることが期待できます。
概要
広島大学大学院医歯薬保健学研究科(薬科学専攻)の杉山政則教授と、元同研究科の的場康幸准教授(現 安田女子大学薬学部)の研究グループは、分光学的解析法とX線結晶構造解析法を用いてメラニンを生成する酵素「チロシナーゼ」の反応機構を明らかにしました。
メラニン色素をつくるStreptomyces属放線菌のチロシナーゼと、チロシナーゼの触媒活性に必要な銅イオンを輸送するためのタンパク質「キャディー」との複合体においては、チロシナーゼの活性中心にキャディーのチロシン残基(Tyr98残基)が存在しています。本研究グループは、兵庫県立大学の研究グループと協働し、質量分析、紫外可視吸収スペクトル、共鳴ラマンスペクトル等の解析技術を駆使して、チロシナーゼに結合した銅イオンが還元された後に酸素分子と結合すると、キャディーのTyr98残基が反応性の高いドーパキノンへと変換されることを明らかにしました。また、X線結晶構造解析を駆使し、Tyr98残基がドーパキノンに変換される詳細な分子機構を明らかにしました。
本研究成果は、「PLOS Biology」オンライン版に掲載されました。
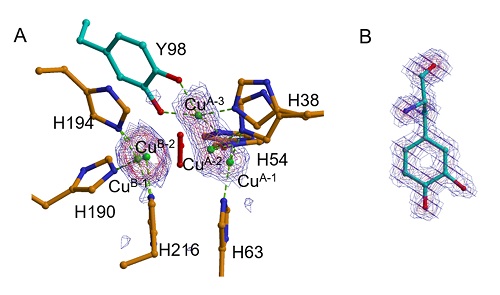
図A 異常分散差フーリエマップ:
CuAがTyr98残基(図中でY98と表示)の水酸基の近く(CuA-3の位置)まで移動している
図B Tyr98残基のオミットマップ:
Tyr98残基が水酸化修飾を受けたことを示している
論文情報
- 掲載雑誌: PLOS Biology (2017年のimpact factor = 9.163)
- 論文題目: Catalytic mechanism of the tyrosinase reaction toward the Tyr98 residue in the caddie protein
- 著者: 的場 康幸1、木原 章吾1、坂東 尚彦1, 吉津 裕成1, 坂口 美幸2, 萱間 紅絵2, 柳澤 幸子2, 小倉 尚志2, 杉山 政則1
1 広島大学大学院医歯薬保健学研究科
2 兵庫県立大学大学院生命理学研究科 - DOI: 10.1371/journal.pbio.3000077
広島大学大学院医歯薬保健学研究科
未病・予防医学共同研究講座
教授 杉山 政則

 Home
Home




