TEL: 082-424-7868
E-mail: takashi-toda*hiroshima-u.ac.jp (*は半角@に置き換えてください)
本研究成果のポイント
- これまで、染色体の分配装置として働く紡錘体微小管形成には微小管モーター蛋白質である5型キネシンの働きが必須であると考えられてきました。しかし、本研究成果により、微小管ポリメラーゼを含む数種の因子が5型キネシンの代わりに紡錘体形成に働くことを初めて明らかにしました。
- 本研究成果により同定した新規の紡錘体形成因子を阻害することにより、がん細胞の増殖を抑えることができると考えられ、副作用の少ないがん治療薬の開発に繋がることが期待されます。
概要
広島大学大学院先端物質科学研究科・健康長寿研究拠点(HiHA)の登田 隆特任教授、湯川格史特任助教らのグループは、今回、カリフォルニア大学との共同研究により、染色体分配装置である紡錘体微小管の形成に新たな因子が働くことを発見しました。
これまで、紡錘体の形成にはキネシンモーター分子の一つである5型キネシンの働きが必須であると考えられていましたが、登田教授らは別の14型キネシンを同時に欠損させた分裂酵母細胞が紡錘体を形成できることを発見しました。
5型および14型キネシン欠損細胞が紡錘体を形成するために必須な因子をさらに探索した結果、6型キネシンおよび微小管ポリメラーゼを含む数種の蛋白質が5型キネシンの代わりに紡錘体形成に働くことを見出しました。
がん細胞は異常な細胞増殖を示しますが、微小管は細胞増殖に必須なため、その阻害剤は抗がん剤として利用されます。ところが、微小管阻害剤は正常細胞に対する副作用が強いという問題があります。本研究で同定した新規の紡錘体形成蛋白質を分子標的にすることで、副作用の少ないがん治療薬を開発できるものと期待されます。
本研究成果は、米国細胞生物学会が発行する国際科学雑誌「Molecular Biology of the Cell」のオンライン版に平成29年10月12日に掲載されました。
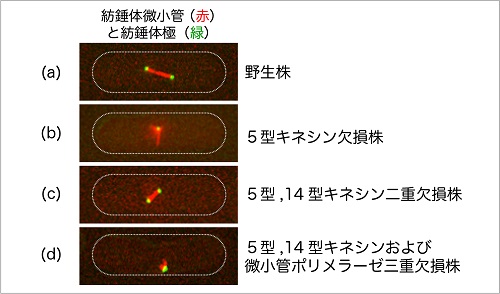
(図1)正常な野生株は双極性の紡錘体微小管を形成します(a)。しかし、5型キネシンを欠損させると単極性紡錘体しか形成できず、染色体分配異常を起こして致死となります(b)。5型, 14型キネシン同時欠損株は双極性紡錘体を形成できますが(c)、さらに微小管ポリメラーゼ欠損を加えた三重欠損株は単極性紡錘体しか形成できず、致死性を示します(d)。従って、微小管ポリメラーゼは、5型キネシンに代わって紡錘体形成に導くと考えられます。
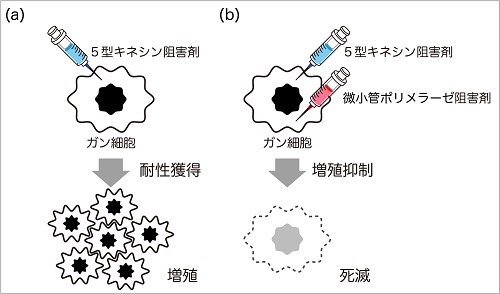
(図2)抗がん剤開発分野においてキネシン阻害剤が注目されていますが、既存の阻害剤を用いた臨床研究では容易にがん細胞が薬剤耐性を獲得してしまうことが大きな課題となっています(a)。本研究で明らかにした新たな紡錘体形成因子に対する阻害剤は、有効ながん治療薬として期待できるほか、キネシン阻害剤との併用投与による一層効果的な抗がん治療法の開発にも貢献できると考えられます(b)。
論文情報
- 掲載雑誌: Molecular Biology of the Cell
- タイトル: A microtubule polymerase cooperates with the Kinesin-6 motor and a microtubule crosslinker to promote bipolar spindle assembly in the absence of Kinesin-5 and Kinesin-14 in fission yeast
- 著者: Masashi Yukawa* and Tomoki Kawakami, Masaki Okazaki, Kazunori Kume, Ngang Heok Tang and Takashi Toda* (*共同責任著者)
- DOI番号: doi:10.1091/mbc.E17-08-0497
- 報道発表資料(349.15 KB)
- 論文掲載ページ(Molecular Biology of the Cellページに移動します)
- 広島大学研究者総覧(登田 隆 特任教授)
- 広島大学研究者総覧(湯川 格史 特任助教)
広島大学大学院先端物質科学研究科・健康長寿研究拠点
特任教授 登田 隆


 Home
Home