本研究成果のポイント
〇先端医療の分野での応用が期待されている細胞外小胞へと有機溶媒や物理刺激を使用することなく、抗がん剤などの疎水性薬剤を導入する手法を開発しました。
概 要
細胞外小胞は細胞が分泌する直径数十nmから数百nm程度の小胞で細胞間の情報伝達媒体としての機能を有していることが知られています。細胞外小胞内部には、タンパク質や核酸、糖鎖、脂質といった生体分子が集積されており、これらの分子を介して、働きかける細胞の種類を選定したり、働きかけた細胞の機能を制御したりと生命現象を高度に制御していることが明らかとなってきました。この細胞外小胞は生体由来の膜小胞であることから、極めて生体適合性に優れるだけでなく、その内部に親水性の薬剤だけでなく疎水性薬剤を導入することができることから、薬剤送達担体としての応用も期待されています。細胞外小胞を薬剤送達担体として利用するためには薬剤の搭載技術の開発が重要となります。水溶性の核酸医薬品やタンパク質医薬品の場合、エレクトロポレーションなど物理的な膜構造の破壊を利用する方法などが用いられてきました。一方で疎水性の薬剤の導入においては有機溶媒の使用や熱や超音波の印加など細胞外小胞の構造を不安定化させうる手法しか取られていませんでした。現在、FDAで認可されている薬剤の多くが疎水性薬剤であることを考えると疎水性薬剤を有機溶媒や物理刺激フリーで搭載する技術の開発は細胞外小胞を基盤とした薬剤送達技術や製剤化技術の発展に大きく貢献できます。
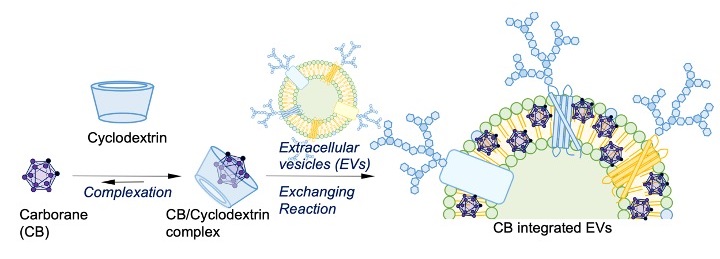
そこで我々は超分子化学的な手法を用いたホスト交換を利用することで疎水性薬剤を極めて効率的かつ均一に細胞外小胞へと導入する手法を開発しました。また、ホウ素クラスターであるカルボランを集積した細胞外小胞はがん放射線療法の一つであるホウ素中性子捕捉療法で高い治療性能を実現しました。
論文情報
Extracellular Vesicles Comprising Carborane Prepared by a Host Exchanging Reaction as a Boron Carrier for Boron Neutron Capture Therapy, ACS Appl. Mater. Interfaces, 16, 47137-47149. (2023).
Riku Kawasaki* Ayano Oshige Nanami Kono Keita Yamana Hidetoshi Hirano Yamato Miura Ryuji Yorioka Kaori Bando Anri Tabata Naoki Yasukawa Masahiro Sadakane Yu Sanada Minoru Suzuki Takushi Takata Yoshinori Sakurai Hiroki Tanaka Dilimulati Yimiti Shigeru Miyaki Nobuo Adachi Ryosuke Mizuta Yoshihiro Sasaki Kazunari Akiyoshi Yoshihide Hattori Mitsunori Kirihata Takeshi Nagasaki Atsushi Ikeda*

 Home
Home





