本研究成果のポイント
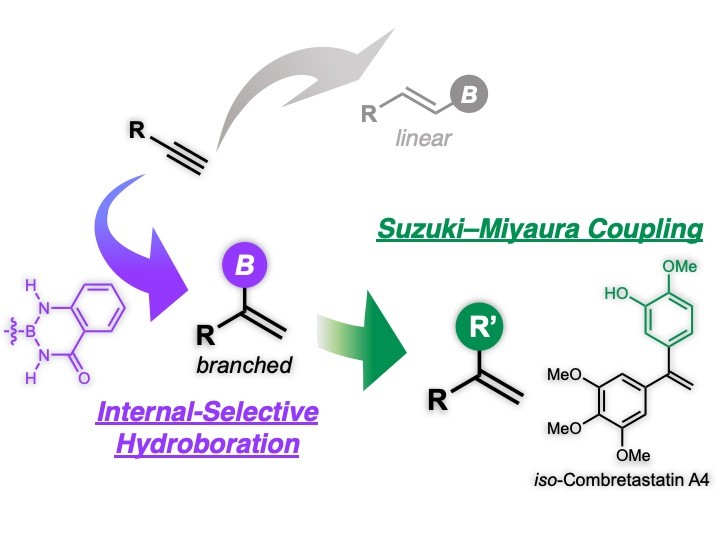
〇鈴木-宮浦クロスカップリング(SMC)反応に利用可能なホウ素部位を末端アルキンの内部炭素に導入することに成功した。
〇「ホウ素のルイス酸性抑制」と「配位子の立体的嵩高さ」が内部選択性の鍵であることを明らかにした。
〇イソコンブレタスタチンA4の短工程全合成を達成した。
概 要
2010年にノーベル化学賞対象となったSMC反応によって、「炭素–ホウ素結合」を足掛かりに有機骨格構築に最も重要な「炭素–炭素結合」を簡便に形成可能となりました。これにより、有機ホウ素化合物は有機材料、農薬、医薬品の製造に不可欠な合成中間体となりました。
有機ホウ素化合物の代表的な合成手法の1つは、末端アルキンのヒドロホウ素化反応です。この反応の位置選択性は、ホウ素のルイス酸性に起因する逆マルコフニコフ則により支配され、三重結合の末端炭素にホウ素が導入された直鎖型ホウ素置換アルケンは、容易に合成することができます。逆マルコフニコフ則は大学有機化学の初歩で取り扱われるほどの一般則であり、選択性を覆し内部炭素へホウ素を導入することは現代有機化学における挑戦的課題でした。
本研究成果は、今後の新しいホウ素導入反応の指針となることはもちろん、多段階を必要とした種々有用分子合成の短工程化にも貢献することが期待されます。
本研究グループは、SMC 反応に利用可能なホウ素部位を末端アルキンの内部炭素に導入することに成功しました。また反応開発過程で、反応の内部選択性の起源が2つあることを明らかにしました。
<銅触媒を用いた末端アルキンの内部選択的ヒドロホウ素化反応の起源>
① ホウ素のルイス酸性抑制度合い
② 配位子の立体的嵩高さ
今回開発したヒドロホウ素化反応とSMC反応を連続的に行うことにより、生物活性分子イソコンブレタスタチンA4の製造工程(従来は4工程必要)をわずか2工程に短縮することに成功しました。

 Home
Home





