広島大学大学院先進理工系科学研究科
教授 安倍 学
E-mail:mabe*hiroshima-u.ac.jp
Tel:082-424-7432
(注: *は半角@に置き換えてください)
本研究成果のポイント
- 量子化学計算により、シクロパラフェニレン骨格(注1)に組み込まれた三重項カルベン(注2)がSOMO-HOMOエネルギー逆転状態(注3)を取ることを発見
- 同様に、いくつかの三重項ジアリールカルベンがSOMO-HOMOエネルギー逆転を起こすことを発見
概要
広島大学、クロアチア・Ruđer Bosǩović Institute、京都大学の研究グループ(研究代表者:広島大学大学院先進理工系科学研究科 教授 安倍学)は、三重項カルベンが計算上SOMO-HOMOエネルギー逆転状態をとりうることを明らかにした。三重項カルベンは、基礎研究やスピン材料への応用の観点から盛んに研究されてきたが、SOMO-HOMO逆転状態についてはこれまで認識されていなかった。本研究成果により、三重項カルベンにおけるSOMO-HOMOエネルギー逆転と物性・反応性との相関の調査等、今後のさらなる発展が期待される。

本研究の成果は、アメリカ化学会の学術雑誌「Organic Letters」に掲載されました。
発表内容
【背景】
SOMO-HOMOエネルギー逆転は、ラジカル(注4)の安定性との相関、酸化による高スピン化学種の発生といった観点から近年多くの関心を集めている。しかしながら、そのような電子配置を示す化学種は少なく、現状では一部の金属錯体や安定ラジカルなどに限られている。SOMO-HOMOエネルギー逆転を引き起こすための分子設計、そこから生まれる新奇的な性質をより深く理解するために、新たな化学種の発見が必要とされている。
【研究成果の内容】
はじめに、シクロパラフェニレン骨格に組み込まれた三重項カルベンnC(n=4-7)がSOMO-HOMOエネルギー逆転状態をとることが量子化学計算により、明らかにされた。
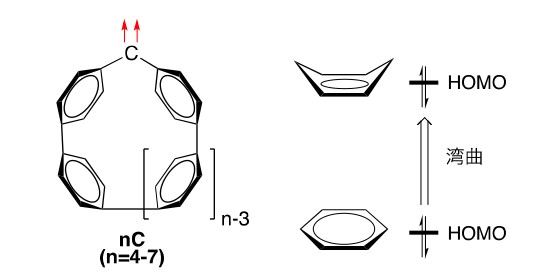
シクロパラフェニレンは、環サイズが小さくなるほど、ベンゼン環が湾曲し、HOMOのエネルギーが高くなることが報告されている。nCにおけるSOMO-HOMO逆転も、シクロパラフェニレン骨格に由来する高いHOMOエネルギーに由来することが本研究によって示唆された。
また、よりシンプルなジアーリルカルベン(下図:F、CH2、O、NH)もSOMO-HOMO逆転を起こすことが明らかになった。
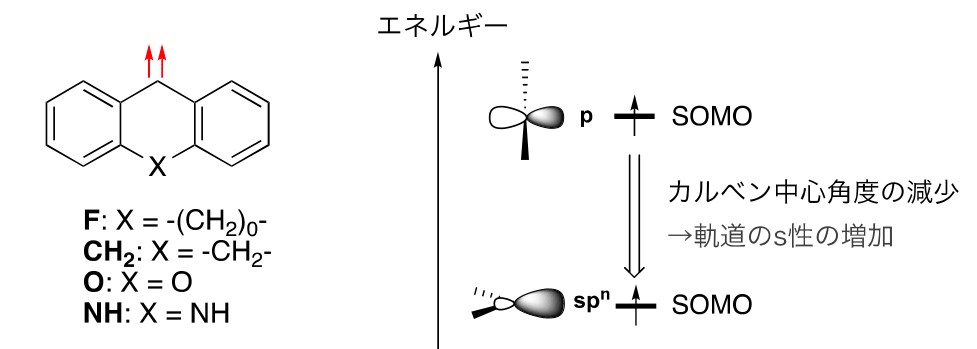
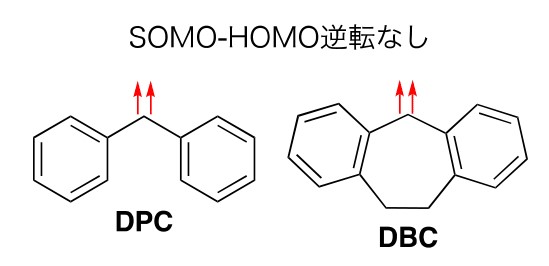
これらのカルベンにおけるSOMO-HOMOエネルギー逆転は、カルベンの中心角度の減少によるSOMO軌道のs性(注5)の増加と、それに伴う軌道の安定化の寄与が大きいと考えられる。F、CH2、O、NHよりも大きなカルベン中心角度をもつジアリールカルベン(下図DPC、DBC)がSOMO-HOMO逆転を示さなかったこともこのことを支持している。
【今後の展開】
本研究で対象としたカルベンの内、F、O、NH、DPC、DBCは既知の化合物である。しかしながら、SOMO-HOMO逆転を起こすと予測されたF、O、NHと通常の電子配置をもつと予測されたDPC、DBCとの間に、SOMO-HOMOエネルギー逆転に由来する性質の違いは見つかっていない。そこで、本研究で同じくSOMO-HOMO逆転が示唆されたnCの実験的発生に今後取り組み、この特異な電子状態と反応性・物性との関係を調査したいと考えている。
用語解説
(※1) シクロパラフェニレン : ベンゼン環がパラ位で環状に繋がった化合物
(※2) カルベン : 2つの不対電子をもつ中性炭素化学種を、カルベンという。不対電子
が対になったものを一重項カルベン、平行になったものを三重項カルベンと呼ぶ。
(※3) SOMO-HOMO逆転: 電子1つを有する分子軌道をSOMOと呼ぶ。一方で、電子2つを有する分子軌道の内、最もエネルギーの高いものはHOMOと呼ばれる。通常これらの軌道のエネルギーは、”SOMOのエネルギー>HOMOのエネルギー”という大小関係をもつ。このエネルギー大小関係の逆転 (SOMOのエネルギー<HOMOのエネルギー)を、SOMO-HOMO逆転と呼ぶ。
(※4) ラジカル : 不対電子をもつ化合物
(※5) s性 : カルベンのSOMO軌道のうちのひとつは、s軌道とp軌道の混成軌道(spn)であると考えることができる。混成軌道のs軌道の割合のことをs性と呼ぶ。s軌道はp軌道よりも安定であるため、s性が高いほど混成軌道が安定になる。
論文情報
- 掲載誌: Organic Letters
- 論文タイトル: SOMO–HOMO Conversion in Triplet Carbenes
- 著者名: Ryo Murata1, Zhe Wang1, Yuki Miyazawa1, Ivana Antol2*, Shigeru Yamago3, and Manabu Abe1*
*Corresponding author(責任著者)
1 Department of Chemistry, Graduate School of Science, Hiroshima University, Hiroshima 739-8526, Japan
2 Laboratory for Physical Organic Chemistry, Division of Organic Chemistry and Biochemistry,Ruđer Bosǩović Institute,10000 Zagreb,Croatia
3 Institute for Chemical Research, Kyoto University, Uji, Kyoto 611-0011, Japan - DOI: 10 .1021/acs.orglett.1c01137

 Home
Home





