本研究成果のポイント
- 菌類(真菌)の仲間において、飽和脂肪酸の一種を過剰に取り込むと、小胞体と呼ばれるオルガネラ(細胞内小器官)の形が変わり、それ以上増殖できなくなる(細胞死を引き起こす)ことを明らかにしました。
- このとき、小胞体は巨大なシート状の異常構造「巨大ERシート」へと変化し、細胞分裂を物理的に阻害します。
- 細胞の新たな機能解明への一助となることや、病原性真菌の増殖を止めるための医薬品・農薬の開発が期待されます。
概要
東京大学大学院農学生命科学研究科の大学院生 星川陽次郎(広島大学大学院統合生命科学研究科 特別研究学生、研究当時)、広島大学大学院統合生命科学研究科の大学院生 代田夏帆と西村慎一 教授、理化学研究所 生命医科学研究センターの津川裕司 客員研究員(東京農工大学大学院工学研究院 教授)、有田誠 チームディレクター(慶應義塾大学薬学部 教授)、理化学研究所 環境資源科学研究センター 部門長の吉田稔 (東京大学 特別教授)らを中心とする研究チームは、菌類の一種である分裂酵母(*1)において炭素数15の飽和脂肪酸(*2)が蓄積すると、細胞内の主要なオルガネラである小胞体(endoplasmic reticulum, ER)(*3)が「巨大ERシート」と名付けた構造体へと変化し(図1、2)、細胞分裂が物理的に阻害されることで、細胞死に至ることを明らかにしました(図3)。
本研究成果は 米国科学アカデミー紀要(Proceedings of the National Academy of Sciences, PNAS)のオンライン版に 2025年5月28日付で掲載されました。
背景
脂肪酸とは、炭素、水素、酸素からできている鎖状の分子で、私たちの身体の中でさまざまな役割を果たしています。例えば、身体を構成する細胞を包んでいる「生体膜」の材料です。また、三大栄養素の一つである「脂質」を作り出すための主要な構成要素であるため、エネルギー源としても大切な分子です。さらに、タンパク質の働きを調整したり、細胞の中で情報を伝える役割をしたりと、多岐にわたる機能を持ちます。
ただ、脂肪酸にはいくつかの種類があるのですが、そのなかでも飽和脂肪酸という脂肪酸を摂取しすぎると、細胞や臓器にさまざまな支障をきたす「脂肪毒性」という現象が起きてしまいます。しかしこの「脂肪毒性」がどうやって起こるのか、その仕組みはまだよくわかっていません。
研究成果の内容
研究グループは、生体膜を標的とする抗真菌化合物(真菌の増殖をとめる物質)を海洋微生物の培養液から探索する過程で、飽和脂肪酸の一種であり炭素数が15のペンタデカン酸が分裂酵母(細胞の真ん中で均等に分裂することで増殖していく酵母)の増殖を阻害することを見出しました。通常の脂肪酸は炭素数2の材料から合成されるため偶数鎖ですが、生体内には微量ながら奇数鎖脂肪酸も存在します。単純な構造の化合物である炭素数15の飽和脂肪酸が酵母の増殖を強く抑制することに興味を持ち、その分子メカニズムの解明研究をスタートしました。
ペンタデカン酸を細胞に添加して顕微鏡で観察すると、オルガネラ(核やミトコンドリアなど、細胞内で特定の役割をもつ細胞内小器官)の一つである小胞体の構造が劇的に変化する様子が見られました(図1、2)。分裂酵母では核の周りと細胞膜の内側に小胞体が存在し、微細なシート状の構造とチューブ状の構造が入り組んだ構造をしているとされますが、ペンタデカン酸を処理すると小胞体が巨大なシート構造へと変化したのです。この異常な構造を研究グループは巨大ERシートと名付けました。さらなる解析を進めたところ、巨大ERシートの形成により細胞分裂の制御が不完全になること、巨大ERシートが細胞分裂部分に挟まって細胞分裂が阻止されることを見出しました(図1、2)。
この新奇な現象の分子メカニズムを明らかにするために細胞内の脂質分子種を網羅的に解析したところ、ペンタデカン酸が細胞膜を構成するグリセロリン脂質(*4)に過剰に取り込まれて飽和脂肪酸の構成割合が高まることが明らかになりました(図3)。重要なことは、細胞の脂質代謝を改変した変異株ではペンタデカン酸が示す効果が、より一般的にみられる炭素数が偶数の飽和脂肪酸の添加でも観察されたことです。これらのことから、分裂酵母で脂肪毒性が引き起こされると、巨大ERシートが形成され、それにより細胞分裂の阻害が起こることが明らかになりました。ペンタデカン酸がより強く脂肪毒性を誘導した理由は、通常の偶数鎖脂肪酸と異なり、分裂酵母の中で代謝変換を受けにくいからだと推定されます。分裂酵母を含む真菌における脂肪毒性の報告は限られており、本研究は巨大ERシートの形成という真菌細胞死の新しい様式を示したものと言えます。
今後の展開
本発見により2つの展開が期待されます。まず、巨大ERシートというユニークな構造の形成や消失の過程を詳細に調べることで、小胞体の構造や機能の理解につながると期待されます。小胞体はタンパク質合成や輸送、脂質代謝、カルシウム貯蔵など、昔から知られている機能に加えて、最近は他のオルガネラの形態や機能の制御など、多様な新しい機能が明らかになりつつある、細胞内の中心的な器官です。巨大ERシートの形成・消失はそのようなオルガネラの機能解明のためのユニークな解析アプローチになると期待されます。
もう一つは、医薬品や農薬の開発への貢献です。ペンタデカン酸が分裂酵母の増殖を阻害するように、病原性真菌の感染を脂肪毒性により抑制する化合物を取得できれば、新しい抗真菌剤のリード化合物になると期待できます。
論文情報
タイトル:Formation of giant ER sheets by pentadecanoic acid causes lipotoxicity in fission yeast
著者:Hoshikawa, Y., Shirota, N., Tsugawa, H., Kimura, S., Matsuyama, A., Yashiroda, Y., Kakeya, H., Arita, M., Iizumi, R., Yoshida, M.* & Nishimura, S.*(*責任著者)
掲載誌:Proceedings of the National Academy of Sciences (PNAS)
DOI:10.1073/pnas.2422126122
用語解説
*1 分裂酵母:均等分裂によって増殖する酵母の総称。本研究で用いたSchizosaccharomyces pombeは真核生物のモデル生物として利用されており、ヒトに保存される生命現象の解析や、抗真菌剤の作用解析などに用いられています。
*2 飽和脂肪酸、不飽和脂肪酸:脂肪酸は炭化水素鎖の端にカルボン酸を持つ分子であり、二重結合や三重結合を持たないものを飽和脂肪酸、持つものを不飽和脂肪酸と呼びます。例えばオリーブ油の主成分であるオレイン酸は不飽和脂肪酸、肉類などに多く含まれるパルミチン酸や本研究で用いたペンタデカン酸は飽和脂肪酸です(図3)。
*3 小胞体(endoplasmic reticulum, ER):小胞体は核の周辺あるいは細胞中に網目状のネットワークを形成しているオルガネラで、タンパク質合成や輸送、脂質代謝、カルシウム貯蔵など、様々なプロセスで機能します。小胞体は2つの膜ドメイン、すなわちシートとチューブから構成され、多様かつ複雑な構造を持ちます。巨大ERシートは本来のシート構造が過度に集合して形成されると考えています。
*4 グリセロリン脂質:細胞膜を構成する脂質分子種のグループ。分子構造には2つの脂肪酸が含まれ(図3)、脂肪酸の種類によって物性が大きく異なります。
図
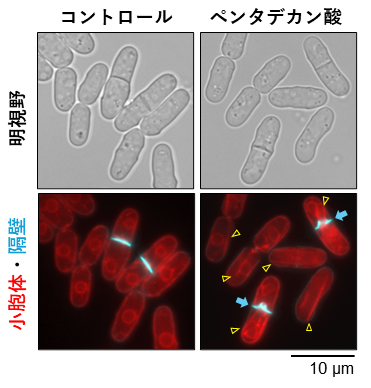
図1.巨大ERシートの蛍光顕微鏡観察像.分裂酵母に小胞体に局在する蛍光タンパク質を発現させ(赤)、また、蛍光色素(青)を添加して細胞分裂時に合成される細胞壁(隔壁)を可視化している。ペンタデカン酸を添加すると巨大ERシートが現れる(黄色の矢頭)。また、隔壁がハの字型に変形し、細胞分裂が邪魔されている細胞が観察される(青矢印)。
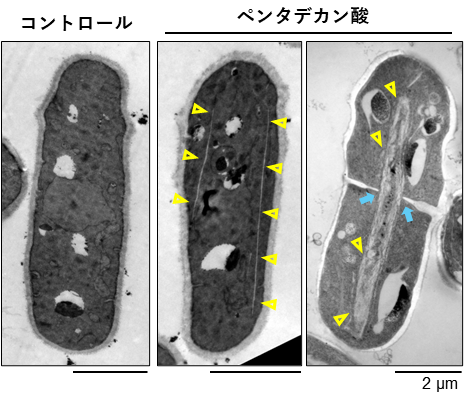
図2.巨大ERシートの電子顕微鏡観察像.透過型電子顕微鏡を用いた観察においても、ペンタデカン酸を処理することで直線状の巨大ERシートの形成が観察され(黄色の矢頭)、それが隔壁形成時に挟まれている様子が見られる(青矢印)
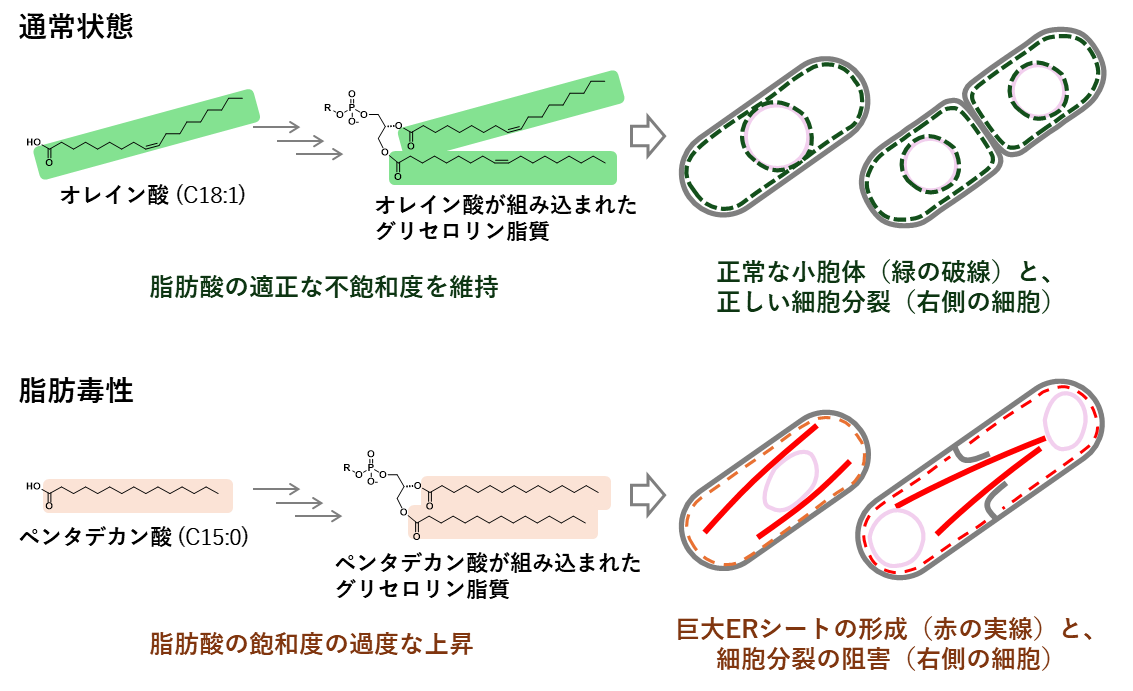
図3.分裂酵母における脂肪毒性発現の概略.通常状態では細胞はオレイン酸のような不飽和脂肪酸を適度に含んでおり、核(ピンク)の周りと細胞辺縁部に正常な小胞体の構造を維持し(緑の破線)、正しく細胞分裂が進行する。ペンタデカン酸のような飽和脂肪酸を過剰に取り込むと脂肪酸の飽和度が上昇し、小胞体(赤の破線と実線)が巨大ERシート(赤の実線)へと変形し、細胞分裂が阻害されることで、脂肪毒性が発揮される。
謝辞
本研究は、以下の支援を受けて実施されました。
日本学術振興会(JSPS)科研費(JP21H02128, JP19H05640, JP23H05473, JP15H05897, JP15H05898, JP20H00495, JP21K18216, JP24K02011, JP17H06401, JP23H04882, JP24H00493, JP21J21126)、文部科学省(MEXT)学術変革領域研究A「潜在空間分子設計」、バイオサイエンスデータベースセンター(JPMJND2305)、RIKEN Pioneering Project “Glyco-Lipidologue Initiative”、 日本医療研究開発機構(AMED)ムーンショット型研究開発事業(JP22zf0127007)、科学技術振興機構(JST)ERATO「有田リピドームアトラスプロジェクト」、京都大学「ジョン万プログラム」.
また、本研究は広島大学から論文掲載料の助成を受けています。
【お問い合わせ先】
〈研究に関すること〉
広島大学 大学院統合生命科学研究科 教授 西村 慎一
Tel:082-424-7930
E-mail:nshin@hiroshima-u.ac.jp
東京大学 特別教授室 特別教授
理化学研究所 環境資源科学研究センター 部門長 吉田 稔
E-mail:yoshidam@riken.jp
〈広報・報道に関すること〉
広島大学 広報室
Tel:082-424-4383
E-mail:koho@office.hiroshima-u.ac.jp
東京大学大学院農学生命科学研究科・農学部
総務課総務チーム 総務・広報情報担当(広報情報担当)
Tel:03-5841-8179、5484
E-mail:koho.a@gs.mail.u-tokyo.ac.jp
理化学研究所 広報部 報道担当
Tel:050-3495-0247
E-mail:ex-press@ml.riken.jp

 Home
Home