研究内容紹介
微生物の生物機能を細胞レベル・分子レベルで解明し、それを応用することを目指している。以下の3つの研究を行っている。
1)微生物がエネルギーを得る仕組について、関連する蛋白質(シトクロムc、ATP合成酵素)の遺伝子発現、構造形成の熱力学、環境適応性等の視点から解明する(三本木)。
2)真核生物である酵母を材料にして、脂質の細胞内輸送・局在の分子機構、細胞機能における役割について解明する。酵母を用いた高効率脂質生産システムの開発も行っている(船戸)。
3)極限環境生物由来タンパク質の環境適応機構の解明とバイオセンサーとしての応用展開(藤井)。
キーワード
エネルギー代謝,タンパク質,酵母,脂質

シトクロムcの高い安定性の分子機構と微生物細胞内での機能に迫る
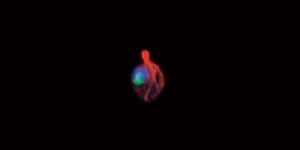
出芽酵母野生株におけるアクチン細胞骨格(赤色),核DNA(青色),核小体蛋白質(緑色)の蛍光顕微鏡観察
最近の業績
Masanari, M., Wakai, S., Ishida, M., Kato, C., Sambongi, Y. (2014) Correlation between the optimal growth pressures of four Shewanella species and the stabilities of their cytochromes c5. Extremophiles, 18, 617-627.
Wakai, S., Kidokoro, SI, Masaki, K., Nakasone, K., Sambongi, Y. (2013) Constant enthalpy change value during pyrophosphate hydrolysis within the physiological limits of NaCl. J. Biol. Chem., 288, 29247-29251.
Fujii, S., Masanari, M., Inoue, H., Yamanaka, M., Wakai, S., Nishihara, H., Sambongi, Y. (2013) High thermal stability and unique trimer formation of cytochrome c´ from thermophilic Hydrogenophilus thermoluteolus. Biosci. Biotech. Biochem., 77, 1677-1681.
Wakai, S., Masanari, M., Ikeda, T., Yamaguchi, N., Ueshima, S., Watanabe, K., Nishihara, H., Sambongi, Y. (2013) Oxidative phosphorylation in a thermophilic, facultative chemoautotroph, Hydrogenophilus thermoluteolus, living prevalently in geothermal niches. Environ. Microbiol. Rep., 5, 235-242.
Yabuki Y., Katayama M., Kodama Y., Sakamoto A., Yatsuhashi A., Funato K., Mizuta K. (2017) Arp2/3 complex and Mps3 are required for regulation of ribosome biosynthesis in the secretory stress response. Yeast,34:155-163.
Palmer EE., Jarrett KE., Sachdev RK., Al Zahrani F., Hashem MO., Ibrahim N., Sampaio H., Kandula T., Macintosh R., Gupta R., Conlon DM., Billheimer JT., Rader DJ., Funato K., Walkey CJ., Lee CS., Loo C., Brammah S., Elakis G., Zhu Y., Buckley M., Kirk EP., Bye A., Alkuraya FS., Roscioli T., Lagor WR. (2016) Neuronal deficiency of ARV1 causes an autosomal recessive epileptic encephalopathy. Hum. Mol. Genet., 25:3042-3054.
Ikeda, A., Kajiwara, K., Iwamoto, K., Makino, A., Kobayashi, T., Mizuta, K. and Funato, K. (2016) Complementation analysis reveals a potential role of human ARV1 in GPI anchor biosynthesis. Yeast. 33:37-42.
Murakami, S., Shimamoto, T., Nagano, H., Tsuruno, M., Okuhara, H., Hatanaka, H., Tojo, H., Kodama, Y., and Funato, K. (2015) Producing human ceramide-NS by metabolic engineering using yeast Saccharomyces cerevisiae. Sci. Rep., Nov 17;5:16319. doi: 10.1038/srep16319.


 Home
Home

