広島大学大学院 医系科学研究科 分子内科学 助教 中島 拓
Tel:082-257-5196 FAX:082-255-7360
E-mail:tnaka*hiroshima-u.ac.jp
(注: *は半角@に置き換えてください)
本研究成果のポイント
- 微生物叢*1の変化はさまざまな病気に影響を与えますが、肺線維症と微生物叢との関係は十分わかっていませんでした。
- 本研究では、消化管の“ありふれたカビ”であるカンジダ*2(Candida albicans)が腸内で増殖すると肺線維症が悪化することをマウス実験で初めて明らかにしました。
- この肺線維症の悪化にはTh17*3・IL-17Aが関与していることを解明しました。腸内でカンジダが増殖すると、まず肺などの離れた臓器にTh17への分化傾向を示すリンパ球が増加し、さらに刺激が加わるとTh17へと分化を遂げサイトカインであるIL-17Aを産生・分泌する、という2段階の制御機構を発見しました。
- さらにIL-17Aは血管内皮細胞に働き「内皮間葉転換*4を誘導する作用があること」を初めて明らかにしました。
- 本研究の成果は微生物叢を標的とした新たな肺線維症治療法の開発につながると期待されます。
概要
広島大学大学院 医系科学研究科 分子内科学の山田 貴弘大学院生、中島 拓助教、服部 登教授らのグループは、ミシガン大学/大阪大学の鎌田 信彦教授と共に「腸内でCandida albicansを増殖させたマウスでは肺線維症が悪化すること」を発見し、そのメカニズムについて新たな知見を蓄積しました。この研究成果は肺線維症を含む難治性疾患に対して、微生物叢を標的とした治療法を開発する上で大きく貢献すると期待されます。
本研究成果は、2023年8月11日に国際学術雑誌である『The Journal of Pathology』オンライン版に掲載されました。
発表論文
- 論文名:Intestinal overgrowth of Candida albicans exacerbates bleomycin-induced pulmonary fibrosis in mice with dysbiosis
- 著者名:Takahiro Yamada1, Taku Nakashima1*, Takeshi Masuda1, Shinjiro Sakamoto1, Kakuhiro Yamaguchi1, Yasushi Horimasu1, Shintaro Miyamoto1, Hiroshi Iwamoto1, Kazunori Fujitaka1, Hironobu Hamada2, Nobuhiko Kamada3, 4, Noboru Hattori1
1:広島大学大学院医系科学研究科分子内科学
2:広島大学大学院医系科学研究科生体機能解析制御科学
3:ミシガン大学消化器内科学
4:大阪大学免疫学フロンティア研究センター
*:責任著者 - 掲載雑誌名:The Journal of Pathology
- DOI:10.1002/path.6169
https://pathsocjournals.onlinelibrary.wiley.com/doi/10.1002/path.6169
背景
肺線維症は肺にコラーゲン沈着を特徴とする呼吸器の難病の一つです。臨床的には抗線維化薬の有効性が示されていますが、その効果は限定的であることから新たな治療法の開発が求められています。
近年、宿主の微生物叢の変化がさまざまな疾患に影響を与えることが報告されており、難治性疾患の病態や新たな治療の標的として期待されていますが、肺線維症と微生物叢との関係は十分理解されていません。我々は微生物叢の変化、特に腸内Candida albicansの増殖が肺線維症の病態に及ぼす影響について、ブレオマイシン*5誘導肺線維症モデルマウスを用いて検討しました。
研究成果の内容
抗菌薬とCandida albicansを飲水ボトルに混ぜて腸内Candida albicansを増殖させたマウス (Candida+) は、Candida albicansを投与しない対照群のマウス (Candida-) と比較して、ブレオマイシン投与によって誘導される肺線維症が悪化しました。Candida+群の肺ではTh17免疫反応が亢進しており、これらのマウスにIL-17Aの中和抗体を投与すると線維化が減弱したことから、この肺線維症の悪化にはTh17・IL-17Aが寄与していると考えられました。この反応は2つの段階によって制御されており、まずCandida albicansが腸で増えるとRORγt (Rorc)というTh17の生存・増殖に重要な役割を持つマスターレギュレーターを発現した「Th17への分化傾向を示すリンパ球」が遠隔臓器でもみられるようになり、次にブレオマイシンの刺激が加わると、刺激部位でTh17へと分化を遂げ、IL-17Aを産生する機序が考えられました。さらに、IL-17Aがこれまでに報告されている作用だけでなく、内皮間葉転換を誘導して線維化を悪化させることを初めて明らかにしました。
今後の展開
本研究は肺線維症においても腸内微生物叢、特にカビである真菌叢と病態との関連がみられることを明らかにした点に特徴があります。今後は、マウス実験の結果がヒトにおいても応用可能かを探り、微生物叢を標的とした肺線維症の新たな治療法開発に結び付けられることが期待されます。
参考資料
本研究の要旨
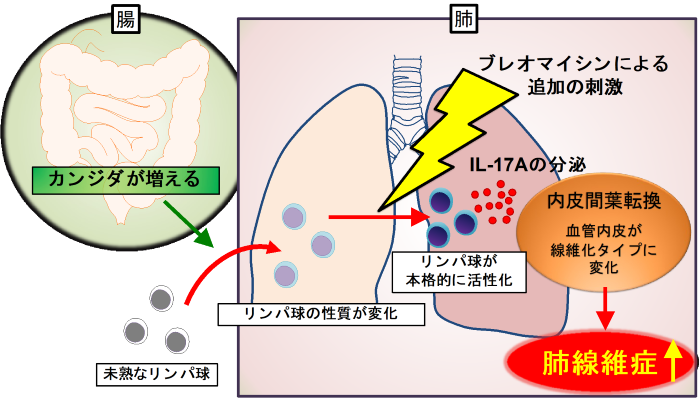
用語解説
*1 微生物叢:膨大な種類・量の微生物(細菌・真菌・ウイルスなど)の集合体。その変化
は免疫細胞やサイトカインの変化を介して、さまざまな影響を及ぼすことが知られる。
*2カンジダ:消化管や皮膚に存在する微生物で、真菌(カビ)の一種。免疫力が正常な人
で問題になることは少ない反面、免疫力が低下した人や抗菌薬を投与された人で問
題になることがある。
*3 Th17:ヘルパーT細胞の一種。IL-17Aというサイトカインを分泌して多くの病気
に関係している。
*4 内皮間葉転換:内皮細胞が間葉系細胞の特性を獲得するプロセス。間葉系細胞には、線維芽細胞などの線維化の進展にかかわる細胞が含まれる。
*5 ブレオマイシン:抗がん剤の一種。マウスの肺線維症モデルを作成する際に一般的に使用される。

 Home
Home



