広島大学大学院医歯薬保健学研究院薬効解析科学研究室
准教授 森岡 徳光(もりおか のりみつ)
TEL:082-257-5312 FAX:082-257-5314
E-mail:mnori@hiroshima-u.ac.jp
平成27年6月25日
難治性疼痛の発症メカニズムを解明
-新しい鎮痛薬開発のための重要発見‐
本研究成果のポイント
- 神経障害性疼痛モデルマウスの脊髄でconnexin43(コネキシン43)が減少していることを発見。
- 脊髄でのconnexin43発現量が減少することが原因となって、痛みの伝達能が亢進している。
- 慢性疼痛が発症した後でも、脊髄のconnexin43発現量を回復させることにより疼痛が緩和。
概要
広島大学大学院医歯薬保健学研究院の森岡徳光(もりおかのりみつ)准教授と張芳芳(ちょうほうほう)(Zhang Fang Fang)研究員らの研究グループは、難治性疼痛モデルマウスを用いて、脊髄の構成細胞の一つであるアストロサイト(※1)に主に発現するタンパク質connexin43が減少し、それに伴って痛みの伝達が亢進していることを明らかにしました。
現在、ガンの終末期、坐骨神経痛、糖尿病、帯状疱疹後などに認められる難治性の疼痛は、患者さんの生活の質(Quality of Life: QOL)を低下させる要因となっています。これらの痛みは、現在汎用されている鎮痛薬であるロキソニンなどの非ステロイド性鎮痛薬やモルヒネなどの麻薬性鎮痛薬が効きにくく、治療が困難であることから、新たな治療薬・治療法の確立が望まれています。
Connexin43は細胞間コミュニケーションに関わるタンパク質であり、痛みの神経伝達に対して重要な役割を果たす細胞であるアストロサイトに主に発現していることが知られています。同研究グループは、マウスを用いた実験により、難治性疼痛の一種である神経障害性疼痛(※2)時の脊髄においてconnexin43発現量が減少し、慢性的な痛みの発生に関与していることを見出しました。またconnexin43の減少により、脊髄での痛み伝達に関与するグルタミン酸の働きが亢進しており、この現象が痛みの慢性化の要因であることを明らかにしました。さらにアデノウイルスベクターを用いた遺伝子導入法(※3)により、減少したconnexin43発現量を回復させることで、疼痛反応が減弱することも証明しました。
これらの結果より、connexin43が難治性疼痛に対する治療標的となることが示され、難治性疼痛に苦しむ多くの患者さんを救う新たな治療戦略を提示する可能性が期待されます。
本研究成果は、平成27年6月24日(日本時間)発行の科学誌「Brain, Behavior, and Immunity」のオンライン版で公開されました。
発表論文
著者
Norimitsu Morioka*, Fang Fang Zhang, Yoki Nakamura, Tomoya Kitamura、 Kazue Hisaoka-Nakashima and Yoshihiro Nakata
* Corresponding author(責任著者)
論文題目
Tumor necrosis factor-mediated downregulation of spinal astrocytic connexin43 leads to increased glutamatergic neurotransmission and neuropathic pain in mice.
掲載雑誌
Brain, Behavior, and Immunity, 2015
DOI番号
10.1016/j.bbi.2015.06.015
研究の背景
神経障害性疼痛に代表される難治性の痛みの治療において、慢性化した痛みを緩和することが重要です。一方、何故痛みは慢性化するのか、そのメカニズムは不明でした。そのため、痛みの慢性化に関わるメカニズムを明らかにすることで、これまでにない新たな鎮痛薬の創製に繋がることが期待されます。本研究では、神経障害性疼痛モデルマウスを用いて、痛みの伝達において重要な組織である脊髄での機能変化に注目しました。特に、痛みの神経伝達機能に関与する細胞であるアストロサイトに発現するconnexin43の発現変化と痛みに及ぼす影響を、生化学的解析ならびに動物行動解析により検討しました。
研究成果の内容
森岡徳光准教授らの研究グループは、坐骨神経を損傷して作成した神経障害性疼痛モデルマウスの脊髄において、対照群と比較してconnexin43発現量が減少することを明らかにしました(図1)。特に痛みの慢性期(神経損傷後1週間から3週間)において、connexin43発現量の有意な減少が認められました(図1)。またRNA干渉法(※4)により脊髄でのconnexin43発現量を人為的に低下させたマウスにおいても、神経障害性疼痛モデルと同様に痛みが発症しました。反対に、アデノウイルスベクターを用いた遺伝子導入法により、脊髄のconnexin43発現量を回復させると、神経障害性疼痛が有意に減弱しました(図2)。
さらに脊髄でのconnexin43発現量の低下により、痛みの伝達能が亢進していることがわかりました。特に痛みの伝達に関与する神経伝達物質であるグルタミン酸の働きが亢進していることを明らかにしました。
また炎症誘発物質である腫瘍壊死因子(tumor necrosis factor: TNF)が脊髄でのconnexin43発現低下を誘発する物質であることも突き止めました。
これら結果は、神経障害性疼痛の慢性化の要因として、脊髄でのconnexin43発現量の低下が関与していることを示唆するものであり、さらにその発現回復を介して難治性の疼痛を緩和できる可能性を提示しています。
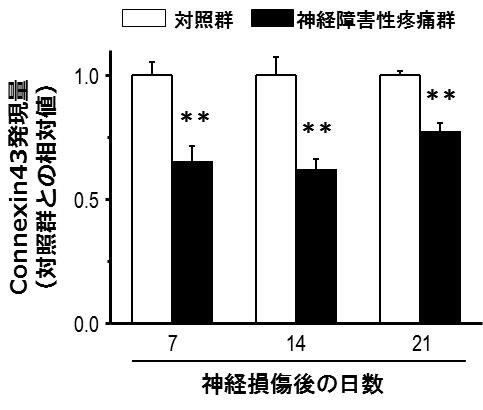
図1. 神経障害性疼痛時の脊髄におけるconnexin43発現量の変化
神経損傷後7、14、21日目の脊髄において対照群と比べてconnexin43発現量が低下しました。
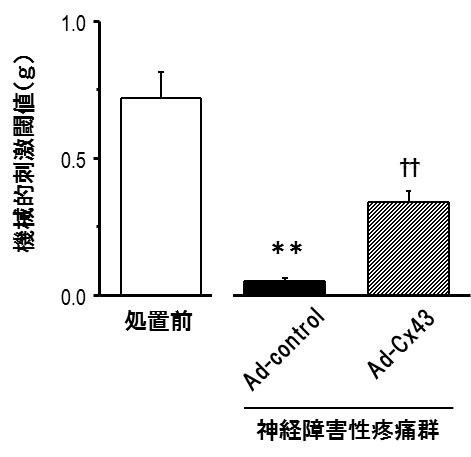
図2. 神経障害性疼痛に対するconnexin43発現量回復による疼痛緩和効果
神経損傷後14日目において、マウス脊髄くも膜下腔内へconnexin43を発現するアデノウイルスベクター(Ad-Cx43)を投与することにより、コントロールアデノウイルスベクター投与群(Ad-control)と比べて疼痛は緩和されました。
(本グラフは、縦軸が低値を示すほど痛みが強い状態であることを示しています)
今後の展開
本研究結果から、connexin43発現量を増加・回復させる薬剤が新たな鎮痛薬候補となる可能性が予想されます。我々はすでに候補物質を同定しており、その有効性について神経障害性疼痛モデルを用いて解析を進めているところです。
用語解説
(※1)アストロサイト:中枢神経系に存在する細胞で、グリア細胞の一つ。神経細胞の機能調節や構造維持に関与している。
(※2)神経障害性疼痛:ガンや物理的傷害による末梢神経及び中枢神経の障害や、機能的障害による慢性疼痛疾患の一種
(※3)アデノウイルスベクターを用いた遺伝子導入法:アデノウイルスが元々持っている細胞進入機構を利用して細胞内に特定の遺伝子を導入、発現させる方法
(※4)RNA干渉法:特定の遺伝子発現を抑制する技術。
広島大学学術・社会産学連携室広報グループ 楠本 記章
TEL:082-424-6762 FAX:082-424-6040
E-mail:koho@office.hiroshima-u.ac.jp
(@は半角に直して送信して下さい。)

 Home
Home





