発表のポイント
● XPRIZE Healthspan (注1)のセミファイナル臨床試験において、PAI-1阻害薬「TM5614」(注2)を高齢者へ4ヶ月投与した結果、生物学的年齢(注3)が平均2〜3歳若返るなど、ヒトの遺伝子、遺伝子修飾(エピゲノム)、タンパク・細胞レベルで抗老化効果を確認しました。
● 免疫、代謝、骨・筋肉、認知・神経生理、凝固・線溶、抗酸化など、広範な改善が確認され、比較的健常な高齢者にも安全に投与可能であることが示されました。
● TM5614は「老化細胞を除去し、種々の加齢に伴う症状を改善できる新たな内服薬(Senolytic drug)候補」として健康寿命の延伸に寄与する可能性が示唆され、XPRIZE Healthspanファイナル試験への申請に向けた重要な臨床データが取得できました。
概要
これまでTM5614は多くのがん患者には投与されてきましたが、比較的健康な高齢者を対象とした臨床試験は初めてです。
東北大学、広島大学、東海大学、株式会社レナサイエンスらは、国際的な長寿コンペティション「XPRIZE Healthspan」のセミファイナル臨床試験(特定臨床研究)を実施しました。本試験では、加齢に伴い発症する疾患(高血圧症、2型糖尿病、慢性腎臓病、高脂血症)を有する50歳以上75歳以下の被験者20例を対象に、TM5614を4ヶ月間投与しました(臨床試験責任医師は張替秀郎東北大学理事・副学長)。その結果、生物学的年齢が平均して2〜3歳若返り、免疫や再生の機能が回復し、老化を促す物質が減少するなど、全身の抗老化を示唆する知見が確認されました。さらに、老化関連microRNA(注4)の減少、抗炎症や代謝改善に関わるタンパク質の変動、免疫細胞および造血幹細胞の機能回復、酸化ストレスマーカーの改善など、遺伝子、遺伝子修飾(エピゲノム)、タンパク、細胞レベルにわたる広範な改善が認められました。また、重大な副作用は確認されず、比較的健康な高齢者に対しても安全に投与可能であることが示されました。
本成果は、老化そのものに介入する内服薬の臨床応用の可能性を示すものであり、健康寿命の延伸に向けた新たな治療戦略として期待されます。今後は、2026年8月のファイナリスト選定を経て、日本、米国、サウジアラビア、台湾との国際共同による大規模臨床試験の実施を目指します。
詳細な説明
研究の背景
XPRIZE Healthspanの公募要項によれば、セミファイナリスト(TOP40)は、最終的な4年間のファイナル臨床試験の実現可能性を支持するための短期間(4週〜8週)、小規模(5~20人)の臨床試験をセミファイナル臨床試験として実施しなければいけません。そこで、東北大学、広島大学、東海大学、株式会社レナサイエンスらは共同で、加齢に伴い発症する疾患(高血圧症、2型糖尿病、慢性腎臓病、高脂血症)を有し、症状が安定している50歳以上75歳以下の20例を対象に、TM5614を4ヶ月間投与する非盲検試験をセミファイナル臨床試験として実施しました(臨床試験責任医師は張替秀郎東北大学理事・副学長)。
投与期間が短期間のため、各種臓器の抗老化作用を評価することは難しいことから、老化、免疫、代謝、骨・筋肉、認知・神経生理、抗酸化、造血幹細胞など、各種臓器の老化に関わる遺伝子、エピゲノム(遺伝子修飾)、タンパク、細胞などのバイオマーカー(注5)の変動を解析しました。
実施医療機関は東北大学、さらに検査などの協力機関として広島大学、東海大学が参加しました。TM5614を4ヶ月間投与した前後の検査が実施できた19名の患者(平均年齢60.4±5.6歳、男性13名、女性6名)を有効性評価の対象とし、TM5614投与を受けた20名の患者を安全性評価の対象としました。
その結果、安全性に関しては、TM5614との因果関係が否定できない有害事象は1例で認められましたが(軽度肝機能異常)、その他の重篤な副作用は出血イベントを含めて確認されませんでした。
また有効性に関して、投与期間は4ヶ月と比較的短い期間でしたが、全身の抗老化を示唆する下記の知見が確認されました。
(1) エピゲノムあるいは遺伝子レベルでの改善
1) 生物学的年齢 (Epigenetic clock)の若齢化
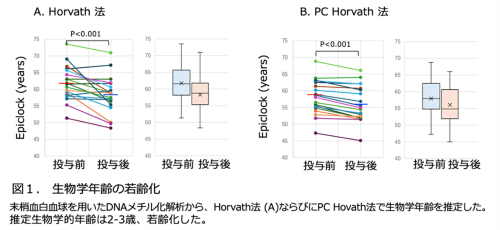
遺伝子 (DNA)のメチル化修飾(エピゲノム)を解析することにより、生物学的年齢を推定することが可能です。白血球を用いたDNAメチル化解析に基づき、Horvath法及びPC-Horvath法(注6)を用いて生物学的年齢を推定した結果、対象者の実年齢(平均60.4歳)に対し推定した生物学的年齢はそれぞれ61.7歳および58.0歳と、実年齢に近い値を示しました。4ヶ月間の投与後における解析では、Horvath法で58.3歳(p< 0.001, 19人中15人で減少)、PC-Horvath法で56.1歳(p< 0.001, 19人中18人で減少)へと有意な若齢化が認められました(それぞれ3.4歳および1.9歳の生物学的年齢の若齢化を確認しました)(図1)。
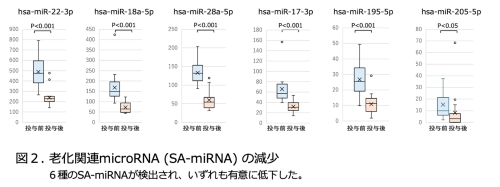
2)老化関連microRNA(Senescence-associated (SA)-miRNA)の減少
microRNA(miRNA)は、遺伝子発現を調節する長さ約20塩基のRNAです。血清中の老化関連senescence-associated(SA)-miRNAを解析したところ、SA-miRNA(miR-22-3p、miR-18a-5p、miR-28-5p、miR-17-3p、miR-195-5p、miR-205-5p)はいずれも有意に低下し、老化を誘導する遺伝子発現制御が軽減したことが示唆されました(図2)。
(2)タンパクレベルの改善
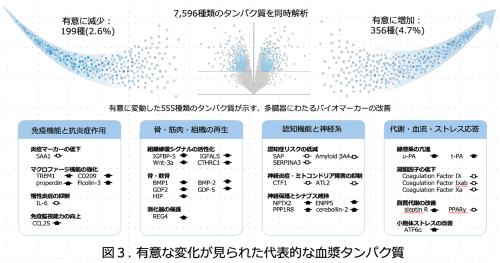
アプタマー(核酸抗体)を用いたソマスキャンアッセイ(注7)により7596個の血漿タンパク質を解析しました。有意に増加したタンパクが 356個(4.7%)、有意に低下したタンパクが199個(2.6%)でした。19人中多くの被験者が同様に変化し、有意な変動が認められたタンパク質が複数見出されました。抗加齢作用と関連する複数のタンパク質の変化が認められ(図3)、抗炎症作用やマクロファージ機能の改善、骨および筋肉組織形成の改善、認知機能および神経生理機能の改善、抗血栓作用、脂質代謝改善、小胞体(ER)ストレス改善など、老化防止に関わる可能性が示唆されました。
(3)細胞レベルでの改善
1)免疫系の活性化
末梢血中の免疫細胞を表面マーカーで分画したところ、ナチュラルキラー細胞(NK細胞)(注8)数の減少(p<0.05, 19人中14人で減少)が確認されました。NK細胞は、がん細胞や老化細胞を除去する自然免疫を担う主要なリンパ球ですが、老化とともに機能が低下し、それを補うために細胞数が増加することが知られています。さらに、樹状細胞(注9)数の増加(p<0.05, 19人中12人で増加)が確認され、老化細胞等に対する免疫監視が向上した可能性が示唆されました。
2)造血幹細胞の機能回復
末梢血中の造血幹・前駆細胞(注10)数は加齢に伴い減少し、造血能力は低下します。末梢血単核球を解析したところ、造血幹・前駆細胞数が有意に増加し (p<0.05, 19人中15人増加)、特に加齢によるリンパ球産生低下の一因とされる多能性前駆細胞MLP(multi-lymphoid progenitor)数が増加しました(p<0.05, 19人中15人増加)。さらに、造血幹・前駆細胞における遺伝子発現をRNA-seq解析(注11)により網羅的に解析したところ、その分化段階を示す遺伝子群が有意に変動し、遺伝子発現が全般的に若齢化していることが示唆されました。
(4)酸化ストレスマーカーの改善
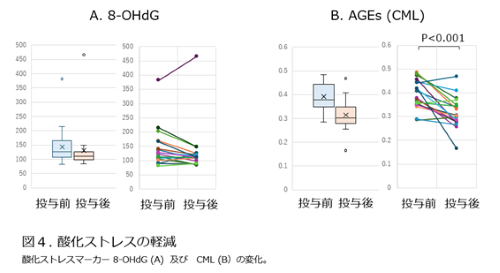
酸化ストレスは、老化と深く関係しています。血清酸化ストレスマーカーである8-OHdG(注12)レベルの減少傾向(p=0.118, 19人中14人減少)が確認されました。また、タンパク質の糖化反応により生成され、老化の指標の1つと考えられる終末糖化産物(advanced glycation end products, AGEs)(注13)であるCML (カルボキシメチルリジン)(注14) の低下が認められました(p<0.01, 19人中16人で減少しました)(図4)。
今後の展開
PAI-1阻害薬TM5614を4ヶ月間投与することにより、エピゲノム(遺伝子修飾)あるいは遺伝子レベルでの改善が認められました。特筆すべきは、生物学的年齢の2〜3歳の若齢化です。タンパクレベルでも、免疫機能、骨・筋肉機能、代謝機能、ならびに認知機能の改善など、抗加齢作用に関わる複数のタンパクの改善が認められました。また、細胞レベルにおいても、免疫細胞、造血幹細胞の機能回復や若齢化が認められ、さらに全身での酸化ストレスの軽減も確認されました。
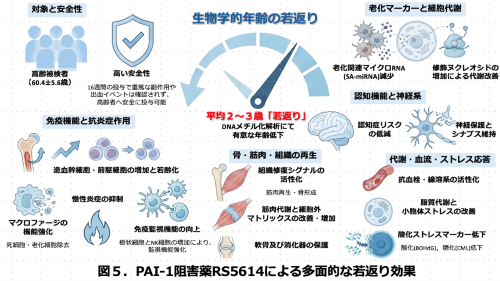
比較的健康な高齢者に対してもTM5614は安全に経口で投与できることが確認されたことだけでなく、4ヶ月間という短期間の投与にも関わらず、免疫、代謝、骨・筋肉、認知・神経生理、抗酸化、造血幹細胞など、広く各種臓器に対して抗老化作用が確認されました(図5)。これらの分子レベルでの変化が、各種臓器の抗老化作用に繋がり、最終的に健康寿命の延伸につながるかどうか、今後さらなる検証が必要です。
今回のセミファイナル試験結果とファイナル試験計画をまとめて、2026年4月にXPRIZE Healthspan評価委員会に提出しました。2026年8月にファイナリスト(TOP10)として採択されれば、ファイナル試験は日本、米国、サウジアラビア、台湾との国際共同臨床試験として実施し、100名以上の高齢者を対象としたプラセボ対照盲検試験で免疫機能、筋肉機能、認知機能を評価する予定です。さらに、TM5614投与によってもたらされる遺伝子(トランスクリプトーム(注15))、エピゲノム、タンパク(プロテオーム(注16))などマルチオミクスを解析することで、老化のバイオマーカーを探索し、より正確な生物学的年齢評価方法を検討する予定です。
従来の医薬品開発は「単一疾患」「単一標的」「明確な評価指標(エンドポイント)」を前提としています。一方、「老化」は加齢(生理的変化)の延長であり「疾患」とは見做されておらず、さらに老化は連続的かつ個体差が大きいため、「老化」を単独の疾患(適応症)として開発することは困難です。そのため、実用化にあたっては規制、臨床試験デザイン、保険償還制度、ビジネスモデルといったさまざまな課題があります。しかし、近年、これまでの古典的な老化介入(食事療法、運動療法、睡眠療法、サプリメントなど)とは異なるエピジェネティック・リプログラミング(細胞若返り)(注17)やセノリティクス(老化細胞除去)(注18)など新たな機序に基づく老化介入(治療法)が提案され、一部では臨床試験も開始されつつあります。
PAI-1阻害薬RS5614はセノリティクスを目的とする内服薬です。老化はエピジェネティック情報、代謝、炎症、幹細胞機能など広範な生体の恒常性が崩れた状態であり、老化に介入する場合、複数経路にまたがる統合的な介入が必要になります。「特定の病態を改善する」のではなく「老化の環境を広く改善し、生体全体のバランスを再構築する」という視点が重要です。老化細胞は免疫系により除去されず蓄積すると、老化関連分泌形質と呼ばれる炎症性サイトカインやケモカインを持続的に放出し、周囲の健全な細胞や組織に慢性炎症を引き起こします。PAI-1阻害薬は、複数経路にまたがり統合的に介入し、崩れた生体全体の恒常性を再構築できる医薬品候補で、老化環境を改善し、老化細胞を除去し、生物学的年齢を若返らせ、種々の加齢疾患を予防・治療できるポテンシャルを有します。
謝辞
本研究には、下記の先生が参加されました:東北大学の張替秀郎教授、宮田敏男教授、田久保圭誉教授、藤井博司教授、片桐秀樹教授、安田聡教授、田中哲洋教授、平澤典保教授、魏范研教授、斎藤芳郎教授、瀧康之教授、山田陽介教授、佐藤大樹講師、長澤将講師、高橋圭助教、進藤智彦助教、河村拓史助教、麻生義則非常勤講師、広島大学の高橋陵宇准教授、田原栄俊教授、平田泰三教授、東海大学の鬼塚真仁教授、八幡崇教授、永井竜児教授
用語説明
注1. XPRIZE Healthspan:健康寿命を延ばすことができた研究チームに対して、総額1億米ドルを支払うという世界的なコンペティション。XPRIZE財団が主催し、人間の老化や長寿に対する治療アプローチに革命を起こし、健康寿命を積極的に10年以上延伸するという挑戦的な課題に取り組むことを目的としています。
https://www.xprize.org/prizes/healthspan
注2. PAI-1(プラスミノーゲンアクチベーターインヒビター1)阻害薬「TM 5614」:PAI-1 は血栓形成に重要なタンパク。TM5614 は、東北大学大学院医学系研究科宮田敏男教授が開発したPAI-1を 阻害する内服薬(医薬品)であり、血栓溶解作用に加えて、がんや老化細胞を除去するための免疫系を亢進する作用を有します。
注3. 生物学的年齢:実年齢とは別に、遺伝子の修飾(DNAメチル化)などに基づいて推定される年齢です。
注4. microRNA:長さ約20塩基のRNAで、それぞれ特定のmRNAに結合して、分解を誘導したり、タンパク質への翻訳を抑制したりして、遺伝子発現を微調整する分子です。
注5. バイオマーカー:体内の状態や病気の状態などを客観的に示す、生体由来の測定可能な物質です。
注6. PC-Horvath法:DNAのメチル化状態を用いて生物学的年齢を推定する方法(第一世代)です。
注7. ソマスキャンアッセイ:特定のタンパク質と結合する核酸分子(アプタマー)を利用し、タンパク質を網羅的に解析する方法です。
注8. ナチュラルキラー細胞(NK細胞):全身をパトロールしながら、がん細胞やウイルス感染細胞などを除去するリンパ球。自然免疫に重要な役割を担っています。
注9. 樹状細胞:血液並びに全身に分布するマクロファージ様の細胞。異物や異常な細胞を識別して除去するとともに、免疫応答を誘導します。
注10. 造血幹・前駆細胞:骨髄や血液中に存在する赤血球、白血球、血小板の元になる細胞、およびその過程にある細胞です。
注11. RNA-seq解析:細胞の中で、今どの遺伝子が、どれくらい働いているかを網羅的に調べる技術です。DNAが体の設計図だとすれば、RNAは現場への指示書です。
注12. 8-OHdG (8-hydroxy-2’-deoxyguanosine):DNAを構成する塩基の一つdeoxyguanosine (dG)の8位が活性酸素種により酸化された 構造を持つDNA酸化損傷マーカーです。
注13. 終末糖化産物(Advanced glycation end products, AGEs):タンパク質と糖が結びつくことで生成されます。この現象を「糖化」と呼び、老化を早める大きな原因の一つとして注目されています。
注14. CML (カルボキシメチルリジン):老化の指標の1つと考えられる終末糖化産物(advanced glycation end products, AGEs)の1つです。
注15. トランスクリプトーム:細胞内に存在する全RNA(転写産物)のこと。不変的な遺伝情報であるゲノム(DNA)に対し、組織や環境、時間経過によってダイナミックに変化するのが特徴です。特定の病気や環境変化において、どの遺伝子が、どの程度活動しているかという生命活動のリアルタイムな状況を網羅的に把握できます。
注16. プロテオーム:特定の細胞や組織で発現しているタンパク質の全集合を指します。不変的な遺伝情報であるゲノム(DNA)に対し、時間や環境、病状に応じてダイナミックに変化するのが特徴です。一つの遺伝子から複数のタンパク質が生じるため、その種類は遺伝子数より遥かに膨大です。生命現象の「今」を直接反映しているため、病気の診断や創薬研究における重要な鍵として注目されています。
注17. エピジェネティック・リプログラミング:DNAの配列を変えずに、メチル化などの遺伝子修飾を書き換えて細胞の運命をリセットする技術です。山中因子(OCT4, SOX2, KLF4)を用い、分化した体細胞をiPS細胞のような万能細胞へ戻す、あるいは若返らせる技術として注目されています。
注18. セノリティクス:体内に蓄積し慢性炎症や病気を引き起こす「老化細胞(ゾンビ細胞)」を除去する医薬品です。老化の根本原因にアプローチし、健康寿命の延伸や加齢性疾患(がんなど)の治療法として期待されています。
【お問い合わせ先】
<研究に関すること>
東北大学大学院医学系研究科
分子病態治療学分野 教授
宮田 敏男(みやた としお)
TEL: 022-717-8157
Email: souyakulab*grp.tohoku.ac.jp
(報道に関すること)
東北大学大学院医学系研究科・医学部広報室
TEL: 022-717-8032
Email: press.med*grp.tohoku.ac.jp
広島大学広報室
TEL: 082-424-3701
Email: koho*office.hiroshima-u.ac.jp
東海大学医学部附属病院事務部事務課(広報)
TEL: 0463-90-2001
Email: prtokai*tokai.ac.jp
株式会社レナサイエンス 広報担当
TEL: 022-727-5070
Email: IR*renascience.co.jp
(*は半角@に置き換えてください)

 Home
Home