広島大学大学院医系科学研究科の丸山博文教授、国立病院機構呉医療センター脳神経内科(広島大学原爆放射線医科学研究所)の倉重毅志医師、徳島大学大学院医歯薬学研究部の森野豊之教授(2021年5月まで広島大学在籍)、和泉唯信教授らの研究グループは、筋萎縮性側索硬化症(ALS、注1)患者の骨格筋での異常に関する研究を行い、ALS患者ではALS診断基準を満たす以前から、骨格筋内にある筋内神経束にALSの病態において非常に重要なタンパク質であるTDP-43(注2)が異常蓄積することを明らかにしました。
ALSは、運動ニューロン(注3)が変性して筋萎縮と筋力低下を来す進行性の病気で、個人差はあるものの、人工呼吸器を使用しなかった場合には発症後2~5年で死に至ります。これまでに治療薬としてリルゾール(経口薬)、エダラボン(点滴注射薬)が保険収載されていますが効果は限定的であり、初発症状を見逃さずにいかに早く治療・ケアを開始するかが重要となります。
一方で、ALSは手足の筋力低下、しゃべりにくさ、飲み込みにくさなどで初発します。ALSを診断するためのバイオマーカー(注4)は確立されておらず、同じような症状の病気はALS以外にもあることから、ALSの診断のためには他の病気が無いことを確認する必要があります.また、ALSは腰椎症、すべり症、腰部脊椎管狭窄症、頸椎椎間板ヘルニア、靱帯骨化症などを合併していることが多いことから、脳神経内科以外の診療科を受診する患者が多いという現状があります。そのため、ALSの診断までに時間を要することが珍しくなく、ALSの進行が速いことも相まって、診療上の大きな問題となっています。
今回の研究では、まず、病理解剖症例(ALS症例10例、非ALS症例12例)の骨格筋組織で、ALSに関連していることが知られているタンパク質の発現を病理学的に評価しました。さらに、その結果を基に、過去に筋生検(注5)を実施した症例のうち、筋疾患と診断されなかった114症例について、タンパク質の発現と生検前後の経過を解析しました。
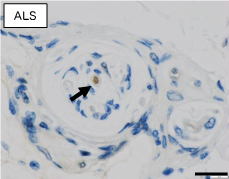
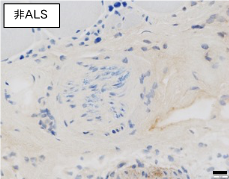
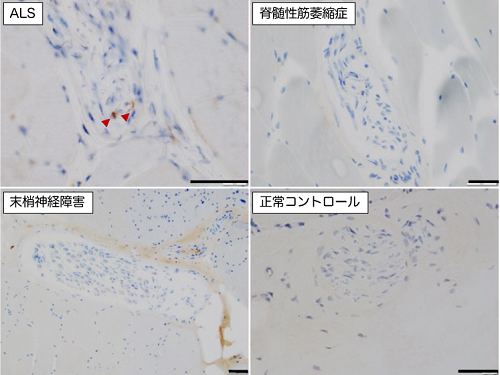
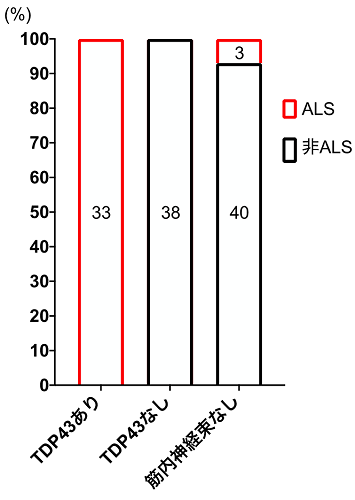
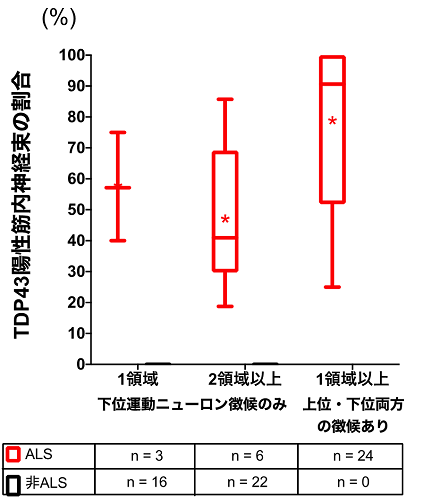
まず、病理解剖症例での検討では、ALS症例の骨格筋内にある筋内神経束にTDP-43が蓄積しており、非ALS症例ではTDP-43は認めませんでした(図1)。また、TDP-43以外のALSに関連したタンパク質の蓄積はALS・非ALSともありませんでした。筋生検症例(図2)では、筋内神経束を含んでいた71例のうち、TDP-43を筋内神経束に認めた33例は全例が最終的にALSと診断されていましたが、筋内神経束にTDP-43が無かった38例は全例がALSを発症していませんでした。生検筋内に筋内神経束を認めなかった43例では3例のみがALSと診断されていました(図3)。筋生検時の症状をゴールドコーストALS診断基準(注6)で分類したところ、ALSの診断基準を満たさない症例であってもTDP-43陽性の筋内神経束を認める症例は最終的にALSと診断されていました(図4)。
本研究の結果から、TDP-43陽性の筋内神経束はALSに極めて特異的に認められ、これまで知られていなかったALSの重要な病理学的特徴と考えられます。今後さらに症例数を増やして確認する必要がありますが、臨床的に強く求められていたALS早期診断のための有用な診断バイオマーカーであると考えています。また、末梢神経の一部である筋内神経束の異常が明らかになったことから、末梢神経でのTDP-43凝集による障害を阻害するALSの新しい治療法開発につながる可能性があります。
本研究成果は、令和4年5月24日午前0時(米国東部標準時5月23日午前11時)に「JAMA Neurology」オンライン版に掲載されました。本研究は日本学術振興会科学研究費助成事業、厚生労働科学研究費補助金 難治性疾患等政策研究事業(難治性疾患政策研究事業)「神経変性疾患領域における基盤的調査研究班」、大樹生命厚生財団、武田科学振興財団、土谷記念医学振興基金の支援を受けて実施したものです。
注1 筋萎縮性側索硬化症(ALS)
運動神経細胞の機能低下による筋萎縮と筋力低下を特徴とする神経変性疾患です。症状は急速に進行し、人工呼吸器装着を行わない場合は発症から死亡までの平均期間はおよそ3.5年です。
注2 TDP-43 (TAR DNA-binding protein of 43kDa)
家族性ALSの原因遺伝子として知られていますが、孤発性ALSの病態においても重要な役割を果たしています。本来は細胞の核内に存在するタンパク質で、TDP-43が運動ニューロンの核から消失して細胞質で異常な凝集体を形成し、さらにこの凝集体によって神経細胞死に至る様々な有害事象が起こることでALSを発症すると考えられています。
注3 運動ニューロン
脳や脊髄に存在し、神経突起を筋肉に延ばし、脳や脊髄からの指令を筋肉に伝える神経細胞です。
注4 バイオマーカー
タンパク質や遺伝子などの生体内の物質で、病状の変化や治療の効果の指標となるものをバイオマーカーといいます。その中でも疾患を特定するために有用なものを診断バイオマーカーと呼びます。
注5 筋生検
筋肉の一部を切り取り、骨格筋の形態的な異常や筋肉の酵素活性などを調べる検査です。
注6 ゴールドコーストALS診断基準
2020年に改訂された新しい診断基準で、進行性の運動機能低下があった場合、それをALSとするものです。具体的には患者さんの症状が、
a)上位および下位運動ニューロンの症状が1身体領域以上にある
b)下位運動ニューロンの症状が2身体領域以上にある
のどちらかを満たしている必要があります。また、ALS以外の病気が検査によって除外される必要があります。
図3 筋生検症例のうち、最終的にALSと診断された割合
図4 ゴールドコーストALS診断基準で分類した筋生検時の下位運動ニューロン徴候(筋力低下など)と上位運動ニューロン徴候(痙性など)の分布

 Home
Home