広島大学大学院統合生命科学研究科 生物工学プログラム
健康長寿学研究室
助教 小川 貴史
Tel:082-424-7763
E-mail:takafumi-ogawa*hiroshima-u.ac.jp
教授 水沼 正樹
Tel:082-424-7765
E-mail:mmizu49120*hiroshima-u.ac.jp
(*は半角@に置き換えてください)
広島大学大学院統合生命科学研究科の小川貴史助教、水沼正樹教授の研究グループと、ハーバード大学・医学部のT. Keith Blackwell教授らの研究グループは、真核生物の成長や寿命を制御する栄養応答因子mTORC1(mechanistic target of rapamycin複合体1)の新規機能の解明に成功しました。
研究グループは、モデル生物の線虫(Caenorhabditis elegans)を用いて、栄養に応答して活性化する栄養応答因子mTORC1の機能を解析し、mTORC1はRNAスプライシングの機能に作用することを発見しました。mTORC1を活性化すると、RNAスプライシングが活性化され、線虫の成長を促進(代謝に関連する遺伝子の発現量の増加を誘導し、同化※5を促進)しました。この現象はヒト細胞でも同様に観察されたことから、ヒトを含む真核生物に共通するメカニズムであることが予想されます。また、これまでmTORC1の抑制は異化※6の誘導によって単細胞生物から哺乳類まで寿命が延長することが知られていましたが、mTORC1の抑制によって低下したRNAスプライシング機能を、RSP-6によって活性化することにより、mTORC1機能低下で誘導される長寿命をさらに延長させることを見出しました(図3)。
本研究成果は、生物の栄養応答や成長の仕組みの解明につながるほか、RNAスプライシングの活性化と従来のmTORC1抑制による寿命延長法を組み合わせることによる新しい寿命延長手法や抗老化薬の開発への応用が期待されます。本研究成果は、国際学術雑誌「Molecular Cell」に11月21日付でオンライン掲載されました。
mTORC1はグルコース、アミノ酸、インスリンなど細胞外の栄養環境を感知する真核生物に存在するタンパク質複合体で、栄養が豊富な状態では同化を誘導して細胞の成長や増殖を促進し、栄養が欠乏した状態では異化を誘導して生命維持にはたらきます。これまでmTORC1の異常な活性化はがん化の原因となる一方、mTORC1抑制剤ラパマイシンは酵母から哺乳類まで寿命を延長することが知られています。近年米国では犬にラパマイシンを与える臨床試験が開始されており、実用的な抗老化標的の可能性が注目されています。また、老化やがんではRNAスプライシング機能の異常も報告されていましたが、mTORC1による成長や寿命制御とRNAスプライシングの関係性は不明でした。
研究グループは線虫のmTORC1の活性が部分的に低下する遺伝子変異体(mTORC1活性低下変異体)を用いて、RNA干渉※7による遺伝子抑制スクリーニングを行い、抑制することにより、mTORC1活性低下変異体が示す成長遅延をさらに悪化させる遺伝子を探索しました。その結果、RNAスプライシングの効率を高める働きを持つ遺伝子のRSP-6などRNAスプライシングに関連する遺伝子を多数同定しました。そこでRSP-6を高発現させ、効率的なRNAスプライシングを活性化させたところ、mTORC1の抑制による成長遅延が回復することを見出しました。
さらに、mTORC1がRNAスプライシングを介して成長を制御するメカニズムを解析しました。栄養に応答してmTORC1はRNAスプライシングを活性化し、選択的スプライシング※2によって、正確なタンパク質情報を持つmRNAの合成が促進され遺伝子発現量が増加することを見出しました。これにより代謝に関連する遺伝子の発現量が増加し、成長を促進することを見出しました(図1)。また、ヒト細胞を用いた解析でも、線虫同様に、栄養に応答したmTORC1はRNAスプライシングを活性化して、成長や代謝に関わる遺伝子発現を促進することを見出しました。このことから、mTORC1によるRNAスプライシングの活性化が成長を促進するメカニズムは、高等生物にも保存されている可能性が示唆されました。
これまでに、mTORC1の活性低下は単細胞生物から哺乳類まで共通して寿命を延長することが知られています。また、RNAスプライシングの活性化は寿命延長との関連性が知られており、その機能異常は老化やがん化との関連が示唆されています。そこで、mTORC1の活性低下によってRNAスプライシング機能が低下したとき、RSP-6を高発現してRNAスプライシング機能を回復させた際の寿命を調べました。その結果、RNAスプライシングの活性化は野生株やmTORC1抑制による長寿命をさらに延長することを見出しました(図2)。これらのことから、mTORC1の下流でRNAスプライシングは成長および寿命延長ともに重要な機能を担っていることがわかりました(図3)。
現在、mTORC1の機能低下による寿命延長が注目されていますが、スプライシングの機能が影響を受けることが分かってきました。今後は、スプライシングの機能を維持させる方策も重要となるでしょう。また、今回発見したRNAスプライシングの活性化と従来のmTORC1抑制による寿命延長法との組み合わせは、既存の寿命延長薬よりも高い寿命延長効果を有することから、本メカニズムを応用した新しい寿命延長手法の開発や抗老化薬などの創薬研究への展開が期待されます。今後も、引き続きmTORC1と相互作用する因子を同定することで、真核生物が栄養に応答して成長を促進する新たなメカニズムの解明が期待されます。
本研究は、日本学術振興会国際的な活躍が期待できる研究者の育成事業(S2902)(小川貴史、水沼正樹)、日本学術振興会・海外学振(小川貴史)、内藤記念科学振興財団(小川貴史)、日本学術振興会・文部科学省科研費若手研究(24K17870)(小川貴史)、日本学術振興会・文部科学省科研費基盤研究(B)(JP22H02260)(水沼正樹)、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(PRIME)「全ライフコースを対象とした個体の機能低下機構の解明」研究開発領域における研究開発課題「S-アデノシルメチオニン(SAM)代謝が関与する寿命延長メカニズムの解明(研究開発者:水沼正樹)(21gm6110029h0004)」および広島大学の支援を受け実施したものです。
※1 線虫(Caenorhabditis elegans):体長1mm程度の線形動物。ライフサイクルが3日、寿命が20日程度と短く、生物の発生や寿命研究においてヒトのモデルとなる生物として利用されている。70%程度の遺伝子がヒトにまで保存されている。
※2 mTORC1(mechanistic target of rapamycin複合体1):真核生物に保存されたリン酸化酵素複合体の一つ。グルコース、アミノ酸、インスリンなど栄養シグナルに応答して活性化すると同化を誘導して細胞成長や細胞増殖を促進する。栄養状態が低下すると活性が低下して異化を誘導することにより生命維持にはたらく。
※3 RNAスプライシング:真核生物にみられる転写後修飾機構のひとつ。DNAから転写されたRNA(pre-mRNA)から不要な配列(イントロン)を切り出し、必要な配列(エクソン)をつなぎ合わせることにより、タンパク質情報を持つmRNAを合成する。この時、一部のエクソンが除去されることもあり、エクソンの組み換えによって多種のmRNAの合成が可能となる。(=選択的スプライシング)
※4 RSP-6:RNAスプライシング遺伝子の一つで、RNAスプライシングが行われる部位を決定し、RNAスプライシングの効率を高めるタンパク質(ヒトSRSF3/SRSF7)
※5 同化:栄養素などの低分子化合物からエネルギーを使用して生体構成物などの高分子化合物を合成する代謝。細胞が栄養を取り込むことで誘導される。
※6 異化:生体構成物などの高分子化合物を低分子化合物に分解し、エネルギーを得る代謝。飢餓状態など栄養状態の低下によって誘導される。
※7 RNA干渉:二本鎖RNAを導入することにより、同一の配列をもつmRNAを切断、分解することにより遺伝子発現を抑制する現象。線虫で最初に報告され、2006年にノーベル賞を受賞。
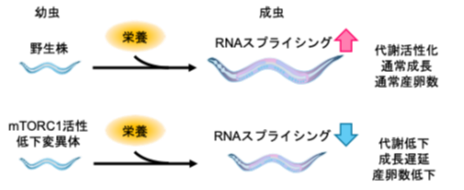
図1: mTORC1によるRNAスプライシングを介した成長制御機構
野生株において、栄養を摂取するとRNAスプライシングが活性化し、栄養代謝、成長、産卵が促進されます。一方、mTORC1活性低下変異体では、RNAスプライシングの活性が低下し、栄養代謝、成長、産卵数も低下します。

図2:RNAスプライシング活性化による寿命延長効果
mTORC1の機能を抑制すると寿命が延長します。また、mTORC1の抑制に加えてRNAスプライシングを活性化すると、mTORC1の抑制による長寿命をさらに延長します。

図3:今回発見したmTORC1を介した新規寿命制御機構
従来mTORC1の抑制によるタンパク質合成低下・オートファジー誘導・ストレス応答が寿命を延長することが知られていました。今回、新たにmTORC1によるRNAスプライシングの活性化は寿命を延長することを発見しました。
以下のサイトから、論文(PDF)が無料でダウンロード可能です。(2025年1月9日まで)
https://authors.elsevier.com/c/1k80f3vVUPRnL5
広島大学大学院統合生命科学研究科 生物工学プログラム
健康長寿学研究室
助教 小川 貴史
Tel:082-424-7763
E-mail:takafumi-ogawa*hiroshima-u.ac.jp
教授 水沼 正樹
Tel:082-424-7765
E-mail:mmizu49120*hiroshima-u.ac.jp
(*は半角@に置き換えてください)
掲載日 : 2024年11月21日
Copyright © 2003- 広島大学